
Badan Pengawas Obat dan Makanan (BPOM) melakukan pengujian terhadap sejumlah obat berbentuk sirop yang terdaftar dan beredar di Indonesia, pascaadanya dugaan sebagai pemicu gagal ginjal akut yang kebanyakan menyerang anak-anak.
Hari ini, Kamis (20/10/2022), BPOM mengumumkan hasil pemeriksaan sampling terhadap 39 bets dari 26 sirop obat yang diduga mengandung cemaran Etilen Glikol dan Dietilen Glikol berdasarkan sejumlah kriteria sampling dan pengujian.
“Kriterianya antara lain, diduga dikonsumsi pasien gagal ginjal akut sebelum dan selama berada di rumah sakit. Diproduksi produsen yang menggunakan empat bahan baku pelarut propilen glikol, polietilen glikol, sorbitol, dan gliserin dengan jumlah yang banyak. Kemudian, diproduksi produsen yang memiliki rekam jejak kepatuhan minimal dalam pemenuhan aspek mutu, dan diperoleh dari rantai pasok yang diduga berisiko mutunya,” kata pihak BPOM dalam keterangan resmi.
Berdasarkan hasil pengujian sampling 39 bets dari 26 sirop obat sampai tanggal 19 Oktober 2022, BPOM menemukan ada lima produk sirop obat dengan kandungan cemaran Etilen Glikol melebihi ambang batas aman.
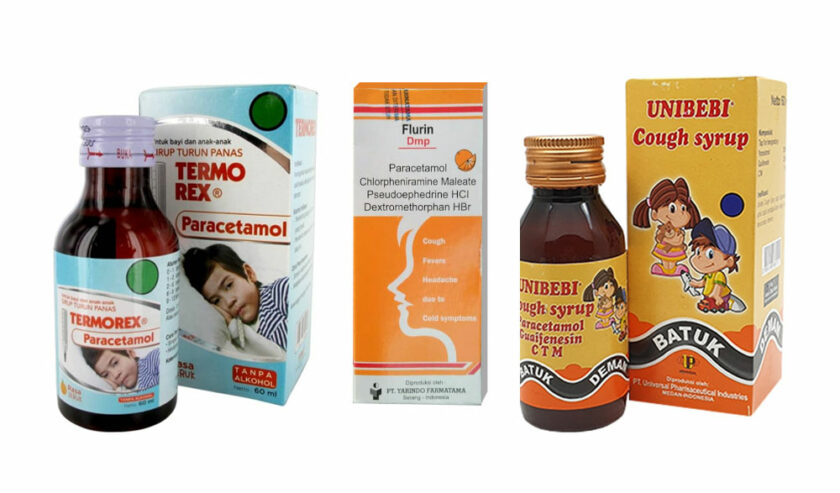
Pertama, Termorex Sirup (obat demam), produksi PT Konimex dengan nomor izin edar DBL7813003537A1, kemasan dus, botol plastik @60 ml.
Kedua, Flurin DMP Sirup (obat batuk dan flu), produksi PT Yarindo Farmatama dengan nomor izin edar DTL0332708637A1, kemasan dus, botol plastik @60 ml.
Ketiga, Unibebi Cough Sirup (obat batuk dan flu), produksi Universal Pharmaceutical Industries dengan nomor izin edar DTL7226303037A1, kemasan Dus, Botol Plastik @ 60 ml.
Keempat, Unibebi Demam Sirup (obat demam), produksi Universal Pharmaceutical Industries dengan nomor izin edar DBL8726301237A1, kemasan Dus, Botol @ 60 ml.
Dan yang kelima, Unibebi Demam Drops (obat demam), produksi Universal Pharmaceutical Industries dengan nomor izin edar DBL1926303336A1, kemasan Dus, Botol @ 15 ml.
Dalam pelaksanaan pengujian terhadap dugaan cemaran Etilen Glikol dan Dietilen Glikol dalam sirop obat, BPOM mengacu pada Farmakope Indonesia dan/atau acuan lain sesuai Undang-Undang Nomor 36 Tahun 2009 tentang Kesehatan, sebagai standar baku nasional untuk jaminan mutu semua obat yang beredar di Tanah Air.
Pihak BPOM menyatakan, sirop obat yang diduga mengandung cemaran Etilen Glikol dan Dietilen Glikol kemungkinan berasal dari empat bahan tambahan.
Yaitu, Propilen Glikol, Polietilen Glikol, Sorbitol, dan Gliserin yang sebetulnya tidak berbahaya atau dilarang dipakai membuat sirop obat.
Merujuk Farmakope dan standar baku nasional, ambang batas aman untuk cemaran Etilen Glikol dan Dietilen Glikol sebanyak 0,5 mg/kg berat badan per hari.
Lebih lanjut, BPOM menyatakan hasil uji cemaran Etilen Glikol belum bisa mendukung kesimpulan penggunaan sirop obat tersebut terkait dengan kasus gagal ginjal akut.
Karena, selain penggunaan obat, masih ada beberapa faktor risiko penyebab gagal ginjal akut seperti infeksi virus, Bakteri Leptospira, dan multisystem inflammatory syndrome in children atau sindrom peradangan multisistem selepas Covid-19.
Menindaklanjuti hasil uji kelima sirop obat dengan kandungan Etilen Glikol yang melebihi ambang batas aman, BPOM memerintahkan industri farmasi pemilik izin edar menarik dari peredaran dan memusnahkan seluruh produknya.
Penarikan mencakup seluruh Pedagang Besar Farmasi, Instalasi Farmasi Pemerintah, Apotek, Instalasi Farmasi Rumah Sakit, Puskesmas, Klinik, Toko Obat, dan praktik mandiri tenaga kesehatan.
Selanjutnya, BPOM memerintahkan semua industri farmasi yang memproduksi sirop obat dengan potensi tercemar Etilen Glikol dan Dietilen Glikol, segera melaporkan hasil pengujian mandiri sebagai bentuk tanggung jawab pelaku usaha.
Selain itu, BPOM menginstruksikan industri farmasi melakukan upaya lain seperti mengganti formula obat dan/atau bahan baku kalau diperlukan.(rid/iss)

 NOW ON AIR SSFM 100
NOW ON AIR SSFM 100









